
首年成效:路线图目标落地见效,八大领域成果显著
过去一年间,FDA 严格落实路线图八大承诺,6 项既定目标如期达成、2 项目标超额兑现,形成了集政策、技术、数据及国际合作于一体的全方位转型支撑架构。
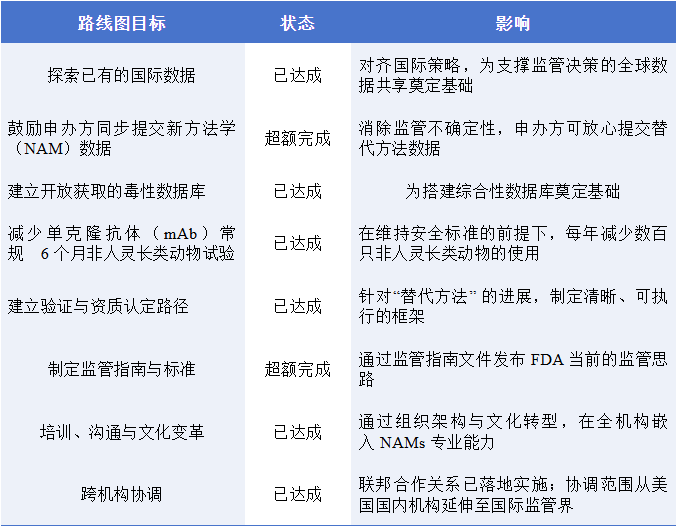
关键成果总结:
1. 政策框架定型:发布单克隆抗体简化非临床安全研究指南,取消6个月非人灵长类动物强制试验,采用“3个月研究+证据权重(WoE)评估”模式即可满足监管要求,每年可减少数百只非人灵长类动物使用量。
2. 监管通道固化:新药创新科学与技术方法(ISTAND)计划转为永久项目,建立药物研发工具(DDT)常态化资质认定机制,累计受理16项创新申报,覆盖肝脏芯片、肾脏芯片、心肌细胞模型等关键技术领域。
3. 验证标准确立:出台NAMs通用验证框架,明确使用场景、人源生物学相关性、技术表征、适用性四大核心原则,将人源方法确立为监管默认标准,有效消除行业应用中的合规不确定性。
4. 数据底座建成:上线可检索NAMs适用数据库,明确替代方法的合规应用场景,将内部审评经验转化为公开指引,切实降低企业申报成本与决策风险。
5. 技术突破落地:认证首个AI药物研发工具AIMNASH,用于代谢相关脂肪性肝炎临床试验病理评分,显著提升评价效率与可靠性;发布肝脏芯片标准化方案,为药物性肝损伤精准评价提供支撑。
6. 跨机构协同深化:与NIH签署合作备忘录,启动ComplementARIE(the Complement Animal Research In Experimentation)计划,整合科研与监管资源,加速NAMs标准化与产业化落地应用。
7. 国际监管对齐:联合欧洲药品管理局(EMA)、日本药品与医疗器械管理局(PMDA)、澳大利亚治疗用品管理局(TGA)达成全球策略共识,构建统一监管语境,降低跨国药物研发的合规成本。
核心价值:科学、产业、伦理三维共赢
本次转型从根本上突破了传统研发模式的瓶颈,实现多维度价值协同跃升:
• 科研层面:以人源模型替代传统动物模型,显著提升药物毒性、免疫原性及药代动力学预测精度,有效降低临床转化失败风险。
• 产业层面:大幅缩短研发周期、削减实验成本、减少重复性试验,加快创新疗法上市进程,提升药物可及性与供给效率。
• 伦理层面:严格践行 3R 原则,显著减少非人灵长类、鲎等实验动物的使用,在满足科研需求的同时,更好地平衡生命伦理与科学发展。
未来路径:持续深化转型,构建全场景NAMs体系
FDA 明确下一阶段八大核心方向,推动监管变革由单点突破迈向全域覆盖:
1.拓展简化试验适用范围,将单克隆抗体的成熟模式推广至生物制品、化学药物及医疗对策产品。
2.搭建动物使用量化追踪体系,以数据驱动实现监管精准优化。
3.优先验证计算毒理学、细胞模型、器官芯片等高频应用 NAMs,全面覆盖关键安全性评价终点。
4.构建国际共享毒性数据库,减少重复试验、提升数据复用与协同效率。
5.完善全终点 NAMs 工具包,补齐发育毒性、慢性毒性等领域替代方法短板。
6.推进多类 NAMs 整合证据权重评价,构建多元互补的人源化安全评价体系。
7.深化 ICCVAM、ICH 等框架下的国际协同,加速全球监管标准统一互认。
8.推动全行业理念与文化转型,提升研发、审评及科研人员对 NAMs 的认知与应用能力。
随着 NAMs 体系不断成熟完善,药物非临床评价将更精准、高效、人道,持续加速创新疗法落地,惠及全球患者,推动药物研发迈向更高质量、更可持续的发展新阶段。
